Trong môn chất hóa học, việc nắm rõ công thức tính mật độ Tỷ Lệ, mật độ mol đó là khóa xe gom chúng ta học viên rất có thể đoạt được từng việc kể từ dễ dàng cho tới khó khăn. Chính vậy nên đấy là những kiến thức và kỹ năng vô nằm trong cần thiết. Trong nội dung bài viết này, hãy nằm trong LabVIETCHEM đi kiếm hiểu về những tính mật độ mol, mật độ Tỷ Lệ và lên đường nhập giải một trong những bài xích tập luyện minh họa rõ ràng, để giúp đỡ chúng ta gia tăng kiến thức và kỹ năng, sẵn sàng hành trang thiệt đảm bảo chất lượng cho tới năm học tập mới mẻ.

Bạn đang xem: Công thức tính nồng độ phần trăm (C%) nồng độ mol Bài tập + Lời giải
Công thức tính C% và công thức tính mật độ mol
Nồng phỏng là gì?
Nồng phỏng là định nghĩa nhằm biểu thị lượng hóa hóa học sở hữu nhập một lếu phù hợp, phần lớn là hỗn hợp. Một số định nghĩa mật độ hoặc gặp gỡ là:
- Nồng phỏng phần trăm
- Nồng phỏng mol
- Nồng phỏng molan: Biểu thị số mol của một hóa học cho tới trước nhập 1kg dung môi
- Nồng phỏng chuẩn: Thường người sử dụng cho tới những phản xạ và hỗn hợp axit – bazo
- Nồng phỏng chủ yếu tắc: Là cơ hội đo mật độ tương tự động như mật độ mol và hiếm hoi Lúc dùng
Nồng phỏng Tỷ Lệ là gì?
Nồng phỏng Tỷ Lệ biểu thị số gam hóa học tan sở hữu nhập 100g hỗn hợp và được ký hiệu là C%.
1. Công thức tính mật độ phần trăm
Qua nghiên cứu và phân tích và demo nghiệm những Chuyên Viên đã mang ra sức thức tính mật độ Tỷ Lệ đúng mực nhất.
Công thức tính C% nhập hóa học:
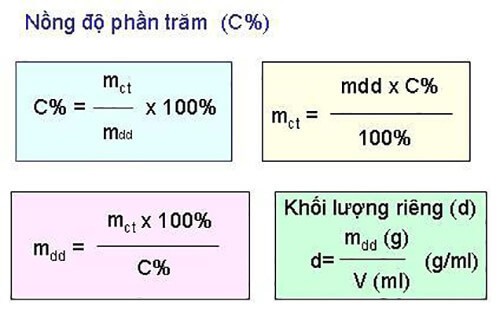
Trong đó:
- C%: Ký hiệu của mật độ phần trăm
- mct: Ký hiệu của lượng hóa học tan
- mdd: Ký hiệu của lượng dung dịch
Công thức tính mdd:
mdd = mct + mdm (trong cơ mdm là lượng của dung môi)
2. Các bước giải bài xích thói quen mật độ phần trăm
Các dạng bài xích thói quen mật độ Tỷ Lệ nhập chất hóa học rất rất nhiều mẫu mã, tuy nhiên bọn chúng đều nên triển khai giải theo đòi quá trình sau đây:
- Bước 1: Khi hiểu đề bài xích tất cả chúng ta rất cần được xác lập được số hóa học sở hữu nhập hỗn hợp, nhất là những số dư của hóa học nhập cuộc phản xạ.
- Bước 2: Tính lượng hỗn hợp sau thời điểm nhập cuộc phảm ứng theo đòi cách thức bảo toàn lượng (tổng lượng hóa học nhập cuộc phản xạ = tổng lượng sản phẩm).
- Bước 3: Tính mct
- Bước 4: sát dụng công thức tính mật độ Tỷ Lệ nhằm giải quyết và xử lý việc.
Áp dụng đích thị 4 bước bên trên đấy là chúng ta trọn vẹn rất có thể tính mật độ Tỷ Lệ rồi. Tuy nhiên, có không ít bài xích tập luyện nó ko cho tới sẵn lượng của những hóa học nên tao rất cần được vận dụng những kiến thức và kỹ năng chất hóa học và được học tập kết phù hợp với công thức tính mật độ Tỷ Lệ nhằm giải việc nhé.
Bài thói quen mật độ Tỷ Lệ của dung dịch
Bài 1: Quý khách hàng hãy tính lượng của NaOH sở hữu nhập 200g hỗn hợp NaOH 15%
Lời giải:
Áp dụng công thức C% = (mct/mdd).100% tao có:
C% = (mNaOH/200).100 = 15 (%)
=> mNaOH = (15.200)/100 = 30 (g)
Trong đó:
- (.) ký hiệu lốt nhân
- (/) ký hiệu lốt chia
Kết luận: Vậy nhập 200g hỗn hợp NaOH 15% sở hữu 30 gam NaOH
Bài 2: Tiến hành hòa tan đôi mươi gam muối hạt nhập nước chiếm được hỗn hợp A sở hữu C% = 10%
a, Hãy tính lượng của hỗn hợp A thu được
b, Hãy ính lượng nước quan trọng cho việc trộn chế
Lời giải:
a, sát dụng công thức C% = (mct/mdd).100% tao có:
mdd=(mmuối.100)/ C% = (20.100)/10 = 200 gam
Kết luận: Vậy lượng hỗn hợp A là 200 gam
b, sát dụng cách thức bảo toàn lượng tao có mnước=mdd - mmuối = 200 - đôi mươi = 180 gam
Kết luận: Vậy nhằm rất có thể trả tan đôi mươi gam muối hạt thì tất cả chúng ta nên cần thiết 180 gam nước muốn tạo đi ra 200 gam dung dịch
Bài 3: Tiến hành hòa tan 3,9 gam Kali nhập 36,2 gam nước tất cả chúng ta chiếm được hỗn hợp B sở hữu mật độ bao nhiêu?
Lời giải:
Ta sở hữu phương trình phản xạ chất hóa học sau
2K + 2H2O -----> 2KOH + H2
Số mol của K = 3,9/ 39 = 0,1 => mol KOH = 0,1 => mol H2O = 0,05
Theo thăng bằng phương trình tao tính được:
mdd = mk + mH2O - mH2 = 3,9 + 36,2 - (0,05.2) = 40 gam
=> sát dụng công thức C% = (mct/mdd).100% tao sở hữu C% = [(0,1.56)/40].100% = 14%
Kết luận: Khi tổ chức hòa tan 3,9 gam Kali nhập 36,2 gam nước đi ra tiếp tục chiếm được hỗn hợp sở hữu mật độ 14%.
Bài 4: Hòa tan 10 gam lối nhập 40 gam nước. Hãy tính mật độ Tỷ Lệ của hỗn hợp chiếm được theo đòi đơn vị chức năng %?
Lời giải:
Khối lượng của hỗn hợp là:
mdd = mdm + mct = 10 +40 = 50 gam
Nồng phỏng Tỷ Lệ là:
C% = (mct/cdd) . 100% = (10/50). 100% = 20%
Vậy mật độ Tỷ Lệ của hỗn hợp chiếm được sau phản xạ là 20%.
Bài 5: Dung dịch HCl sở hữu mật độ là 36%. Tính lượng HCl sở hữu nhập 200g dung dịch
Lời giải:
Xem thêm: c%C3%A1t trong tiếng Tiếng Anh - Tiếng Việt-Tiếng Anh
Nồng phỏng phần trăn hỗn hợp là:
C% = mct/mdd . 100%
=> mct = (C%.mdd)/100%
Vậy lượng hóa học tan HCL là: mHCl = (36%.200)/100% = 72 gam.
=> Các bài xích tập luyện về => Phương trình nhiệt độ phân KClO3 (muối Kali Clorat)
Một số cảnh báo Lúc tính mật độ Tỷ Lệ của dung dịch
- Phải hiểu đề kĩ nhằm hiểu rằng đúng mực những bộ phận tiếp tục cho tới, xác lập được cần thiết đo lường và tính toán những bộ phận nào là.
- sát dụng đích thị công thức tính nhằm tách những sai lầm đáng tiếc ko quan trọng.
- Tính những tài liệu nên cẩn trọng, tách những sơ sót ko xứng đáng sở hữu.
Nồng phỏng mol không giống mật độ Tỷ Lệ như vậy nào?
Nồng phỏng Mol là gì?
Nồng phỏng mol của hỗn hợp cho tới tất cả chúng ta biết số mol hóa học tan sở hữu trong một lít hỗn hợp là từng nào.
Công thức tính mật độ mol
Ngoài công thức tính mật độ Tỷ Lệ thì công thức tính mật độ mol cũng khá cần thiết và xuất hiện tại nhiều trong số bài xích tập luyện.
1. Công thức tính mật độ mol theo đòi khối lượng
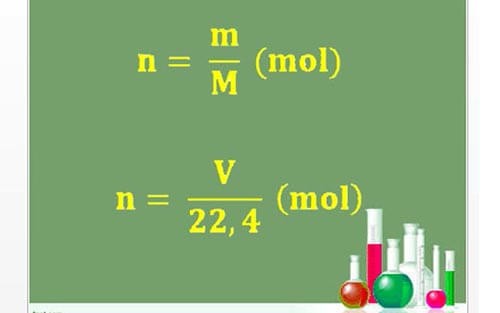
Trong đó:
- n: ký hiệu số mol
- m: lượng của hóa học đó
- M: Khối lượng mol của hóa học cơ (có sẵn nhập bảng tuần trả hóa học)
- V: Thể tích (đktc)
2. Cách tính mật độ mol
Nồng phỏng mol sở hữu ký hiệu là CM và được xem theo đòi công thức
CM=n/Vdd
- CM: ký hiệu của mật độ mol
- n: Ký hiệu số mol hóa học tan
- V: Ký hiệu thể tích dung dịch
3. Bài thói quen mật độ mol
Bài 1: 16 gam NaOH sở hữu nhập 200 ml hỗn hợp, hãy tính mật độ mol của dung dịch
Lời giải:
- Ta thay đổi 200 ml = 0,2 lít
- nNaOH = 16/ 40 = 0,4 mol
=> sát dụng công thức tính mật độ mol CM=n/Vdd tao có
CM = n/ V = 0,4/ 0,2 = 2M
Kết luận: Nồng phỏng mol của hỗn hợp là 2M
Bài 2: Hãy tính lượng H2SO4 sở hữu nhập 50 ml hỗn hợp H2SO4 2M
Lời giải:
Áp dụng công thức tính mật độ mol CM=n/Vdd tao có
nH2SO4 = CM.V = 0,1 mol
=> mH2SO4 = 0,1.98 = 98 gam
Kết luận: Trong 50 ml hỗn hợp H2SO4 sở hữu 98 gam H2SO4 .
Bài 3: Hãy tính lượng hóa học tan cần thiết dùng để làm điều chế 2,5 lít hỗn hợp NaCl 0,9M
Lời giải:
Áp dụng công thức tính mật độ mol CM=n/Vdd tao có
nNaCl = CM.V = 2,5 . 0,9 = 2,25 mol
=> mNaCl = 2,25 . (23 + 35,5)= 131,625 gam
Bài 4: Hãy tính số mol và số gam hóa học tan tỏng 1 lít hỗn hợp NaCl 0,5M
Lời giải:
Vdd = 1 lít, CM = 0,5M
=> nNaCl = CM.V = 1. 0,5 = 0,5 mol
=> mNaCl = m = n.MNaCl = 0,5 . (23 + 35,5)= 29,25 gam
Mối mối quan hệ thân ái mật độ Tỷ Lệ và những mật độ hỗn hợp khác
Giữa mật độ Tỷ Lệ và mật độ mol
CM = (10 x d x C%) / M
Trong đó:
- M: lượng phân tử hóa học tan.
- CM: mật độ mol của hỗn hợp.
- d: lượng riêng biệt của hỗn hợp.
- C%: nồng phỏng phần trăm của hỗn hợp.
Giữa mật độ Tỷ Lệ và mật độ đương lượng
Đương lượng là đơn vị chức năng được dùng nhằm thống kê giám sát tài năng 1 hóa học kết phù hợp với 1 hóa học không giống. Nồng phỏng đương lượng biểu thị số đương lượng gam hóa học tan chứa chấp nhập 1l hỗn hợp. Công thức đối sánh thân ái mật độ đương lượng và mật độ Tỷ Lệ được màn biểu diễn như sau:
CN = (10 x d x C%) / D
Trong đó:
- D: đương lượng gam
- d : lượng riêng biệt của hỗn hợp.
- CN: mật độ tương tự của dung dịch
- C%: nồng phỏng phần trăm của hỗn hợp.
Tính toán tỷ trọng Tỷ Lệ tập luyện trung
- Tỷ lệ Tỷ Lệ mật độ cho tới tao biết sở hữu từng nào bộ phận hoạt hóa học rõ ràng sở hữu nhập hoặc rất cần được sở hữu nhập một biện pháp tổng thể nào là cơ.
- bằng phẳng cơ hội bịa số loại nhất lên bên trên số loại nhị, mật độ Tỷ Lệ được biểu thị là 1:100, 1:200,… rất có thể quy đổi trở thành 1 phần.
- Trong 1 phần Solute (thuốc) sở hữu 100 phần mẻ, 1/100 dung môi.
Hy vọng chúng ta học viên rất có thể ghi ghi nhớ được công thức tính mật độ phần trăm (C%) và công thức tính mật độ mol (CM) và đạt thành phẩm đảm bảo chất lượng nhập kỳ đua. Tham khảo thêm thắt nhiều công thức chất hóa học không giống bên trên trang web trieungoinhaxanh.com.vn.
Xem thêm: Minh Tân - Hình ảnh thời tiết trực tiếp qua vệ tinh
XEM THÊM:
>>> Cách tính đương lượng và ấn định luật đương lượng nhập hóa học
Tìm kiếm:
- công thức quy đổi mật độ mol sang trọng mật độ phần trăm
- tính mật độ Tỷ Lệ những hóa học nhập hỗn hợp sau phản ứng
- bài thói quen mật độ Tỷ Lệ lớp 9 sở hữu Lời giải












Bình luận